2022年12月29日,马秋富教授和他的博士后祁鲁和林星宏在 Neuron 发表了文章Spinal VGLUT3 lineage neurons drive visceral mechanical allodynia but not sensitized visceromotor reflexes,研究了来自肠道的内脏性疼痛。该文同样指出存在不同类型的脊髓神经元,用来驱动和肠道相关的防御反应和情感疼痛。此发现再次呼吁, 需重新审视关于如何测量情感性痛的动物行为。
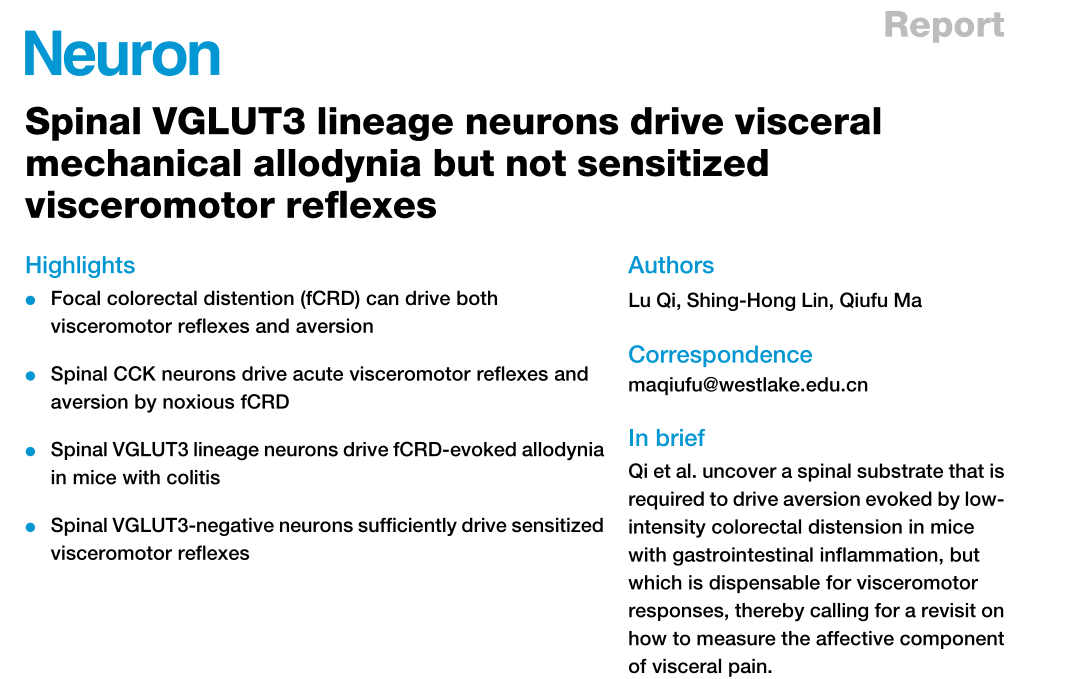
来自内脏器官的疼痛是最普遍的临床问题之一。譬如,10-25%人口患肠易激综合征(Irritable Bowel Syndrome,IBS),目前仍缺乏有效的治疗,导致病人患有长期的慢性疼痛。尽管如此,与皮肤疼痛相比,内脏疼痛的研究还相当缺乏。1988 年,Ness 和 Gebhart 引入了两种方法来研究由结直肠扩张(colorectal distension,CRD) 引起的伤害感受和情感性疼痛。对CRD引起的伤害感受, 他们通过腹部肌肉收缩的肌电图记录来测量,称之为内脏运动反应 (visceromotor response, VMR)。对情感性疼痛的体验, 他们通过实时条件位置回避学习 (the real-time step-down avoidance learning assay) 来测量。
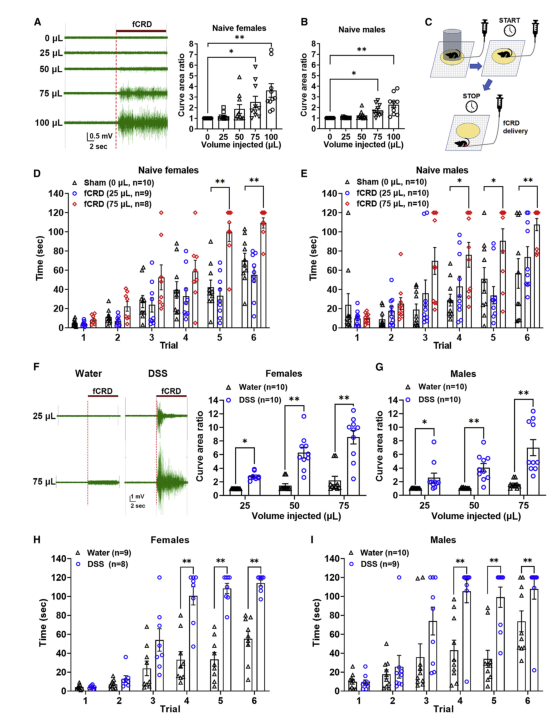

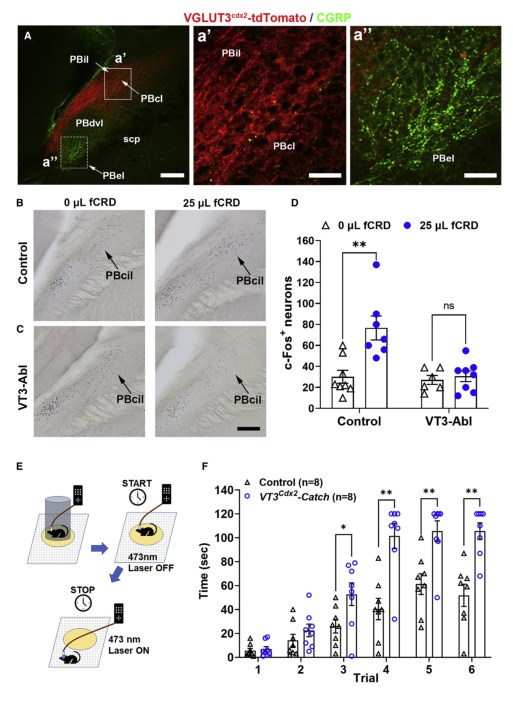
他们发现,在患有胃肠道炎症的野生型小鼠中,低阈值CRD足以引起实时条件位置回避,证明炎症可以引起机械性异常性疼痛。但在敲除了脊髓 VGLUT3 谱系神经元的小鼠,这种低阈值CRD无法诱导实时条件位置回避,证明情感性内脏疼痛的消失。相反,炎症引起的超敏VMR不受影响,表明不属于VGLUT3 谱系的脊髓神经元可以驱动被敏化的内脏运动反射。他们进一步发现VGLUT3 谱系脊髓神经元投射到外侧臂旁核的内核(the internal-lateral parabrachial nuclei, PBil)。之前研究已揭示PBil将身体损伤诱发的感觉信息传递到内侧丘脑核,继而传递到前扣带皮层并驱动情感性疼痛的体验。光遗传学刺激PBil 附近的来自脊髓VGLUT3 谱系神经元的末稍可以充分地驱动实时条件位置回避,但不足以驱动内脏运动反射。这些研究指出存在不同类型的脊髓神经元,用来驱动和肠道相关的防御反应和情感性疼痛。

脊髓VGLUT3 谱系神经元可能代表驱动机械异常性疼痛的会聚节点。这些神经元的一个子集位于深层椎板中,形成多突触通路,将来自皮肤 Ab-LTMR 的输入中继到浅层椎板中的疼痛传递神经元,并且此类输入通常通过前馈抑制进行门控。神经损伤后,Ab-LTMR 输入获得激活 VGLUT3 神经元并驱动一种临床相关神经性疼痛的能力:通过皮肤区域的触觉刺激引起的吗啡抗性动态异常性疼痛。最近的单细胞基因表达谱显示许多结直肠 DRG 神经元表达 Piezo2,一种低阈值机械门控离子通道。在GABA 和甘氨酸受体阻断后,低强度 fCRD 以 VGLUT3 神经元依赖性方式产生厌恶,表明从结直肠传入神经到脊髓 VGLUT3 神经元的输入也被门控通过前馈抑制。未来的研究将旨在确定 DSS 诱导的炎症是否会导致抑制性输入减少和/或兴奋性输入增加,这样低阈值结直肠扩张可以充分激活 VGLUT3 神经元,然后激活驱动情感疼痛的传递神经元。内脏痛的表现通常伴随着涉及的皮肤机械超敏反应。这种超敏反应在 VGLUT3Lbx1-Abl 小鼠中再次被消除。因此,脊髓 VGLUT3 神经元代表了一个有吸引力的细胞靶标,用于治疗源自皮肤和内脏组织的异常性疼痛。